KALOR
Energi panas yaitu, bentuk energi yang berubah menjadi kalor. Energi panas dapat muncul karena terjadinya perubahan bentuk energi, seperti pada reaksi energi kimiawi matahari yang mengakibatkan munculnya api serta panas yang dapat berpindah secara radiasi...
Pengertian kalor
Kalor yaitu, perpindahan energi dari benda yang bersuhu tinggi ke benda yang bersuhu rendah. Secara alami, kalor selalu berpindah / mengalir dari benda yang besuhu tinggi (panas) ke benda yang bersuhu lebih rendah (dingin).
Rumus dan satuan kalor
Satuan ukur kalor yaitu kalori. Satu kalori adalah jumlah energi panas yang dibutuhkan untuk menaikkan suhu 1 gram air menjadi 10C. Namun,Dalam SI satuan kalor ialah joule, 1 kalori = 4,2 joule, 1 joule = 0,24 kalori
Rumus Kalor
Keterangan :
Q : banyaknya kalor yang diperlukanr (J)
m : Massa Benda (kg)
c : Kalor Jenis (J Kg oC)
ΔT : Perubahan Suhu (oC)
m : Massa Benda (kg)
c : Kalor Jenis (J Kg oC)
ΔT : Perubahan Suhu (oC)
Kalor dan Perubahan Pada Benda
Kalor Dapat Mengubah Suhu Zat
Pada dasarnya , setiap benda yang memiliki suhu lebih dari nol, maka benda tersebut memiliki Kalor. Kandungan kalor inilah yang menentukan berapa suhu dari benda tersebut. Apabila sebuah benda dipanaskan, maka benda tersebut menerima tambahan kalor sehingga suhunya jadi meningkat. Sedangkan apabila benda tersebut didinginkan maka benda tersebut melepaskan kalor sehingga suhunya jadi menurun.
Kalor Dapat Mengubah Wujud Zat
beberapa benda jika tambahkan kalor dalam satuan tertentu, benda tersebut akan mengalami perubahan wujud. Contohnya; ketika es dipanaskan (diberi kalor) maka es (dalam wujud padat) itu akan berubah menjadi air ( dalam Wujud cair), dan apabila pemanasan terus dilakukan maka air tersebut juga akan menjadi
Gas. Titik dimana suatu zat akan berubah menjadi Zat Cair dikenal dengan istilah Titik Cair atau Titik Lebur benda.
Kalor Jenis dan Kapasitas Kalor
Menrut hasil penelitian jika kalor diberikan pada dua jenis benda yang berbeda, maka akan menghasilkan suhu yang berbeda pula, misalnya minyak dan air dipanaskan dengan suhu yang beasarnya sama, maka minyak akan mengalami perubahan suhu 2 kali lebih besar dibandingkan air. Ha l Ini dapat terjadi karena benda tersebut memilki kalor jenis yang berbeda.
| Zat | Kalor Jenis | |
| Kal/g oC | J/Kg oC | |
| Air | 1,00 | 4200 |
| Air Laut | 0,93 | 3900 |
| Alkohol | 0,55 | 230 |
| Minyak Tanah | 0,52 | 220 |
| Raksa | 0,033 | 140 |
| Es | 0,595 | 2500 |
| Alumunium | 0,214 | 900 |
| Kaca | 0,16 | 670 |
| Besi | 0,11 | 460 |
| Tembaga | 0,093 | 390 |
| Kuningan | 0,9 | 380 |
| Perak | 0,056 | 230 |
| Emas | 0,031 | 130 |
Apa itu kalor jenis?
kalor Jenis Benda yaitu, banyaknya jumlah kalor yang dibutuhkan untuk menaikkan suhu 1 kg massa suatu benda menjadi 1 derjat celcius. Satuan dari Kalor Jenis yaitu Kalori / GramoCelcius , dalam Sistem Internasional ditetapkan dengan Joule / KilogramoCelcius. Kalor Jenis dapat dirumuskan sebagai berikut
Keterangan :
Q : Kalor (J)
m : Massa Benda (kg)
c : Kalor Jenis (J Kg oC)
ΔT : Perubahan Suhu (oC)
m : Massa Benda (kg)
c : Kalor Jenis (J Kg oC)
ΔT : Perubahan Suhu (oC)
Sedangkan kapasitas kalor yaitu jumlah kalor yang dibutuhkan untuk menaikkan suhu suatu zat menjadi 1 derajat Celcius. Jika kalor Q menghasilkan suhu sebesar t maka kapasitas kalor dapat dirumuskan sebagai berikut;
Contoh Soal Kalor
2 kg air dari suhu 24°C dipanaskan menjadi 90°C. Jika kalor jenis 4.200 Joule/kg°C, maka kalor yang diterima air adalah …
A. 336.000 Joule
B. 259.200 Joule
C. 554.400 Joule
D. 543.600 Joule
Pembahasan
Diketahui :
Massa air (m) = 2 kg
Suhu awal (T1) = 24°C
Suhu akhir (T2) = 90°C
Kalor jenis air (c) = 4.200 Joule/kg°C
Ditanya : Kalor (Q) yang diterima air adalah….
Jawab :
Kalor :
Q = m c ΔT
Q = (2 kg)(4.200 Joule/kg°C)(90°C – 24°C)
Q = (132)(4.200 Joule)
Q = 554.400 Joule
Jawaban yang benar adalah C.
Asas Black
Asas Black adalah hukum yang menyatakan bahwa untuk semua pertukaran energi panas (kalor), maka kalor yang diterima materi bersuhu lebih rendah akan sama besar dengan kalor yang dilepas oleh materi bersuhu lebih tinggi. Secara matematis, Asas Black dinyatakan sebagai berikut.
Jika terdapat dua materi dengan suhu berbeda dicampurkan menjadi satu, asas black dapat digunakan untuk mengetahui suhu akhir campuran. Penerapannya secara matematis adalah sebagai berikut.
Keterangan:
m1 = Massa materi bersuhu lebih tinggi
c1 = Kalor jenis materi bersuhu lebih tinggi
T1 = Suhu materi bersuhu lebih tinggi
m2 = Massa materi bersuhu lebih rendah
c2 = Kalor jenis materi bersuhu lebih rendah
T2 = Suhu materi bersuhu lebih rendah
Tm = Suhu akhir campuran
c1 = Kalor jenis materi bersuhu lebih tinggi
T1 = Suhu materi bersuhu lebih tinggi
m2 = Massa materi bersuhu lebih rendah
c2 = Kalor jenis materi bersuhu lebih rendah
T2 = Suhu materi bersuhu lebih rendah
Tm = Suhu akhir campuran
Contoh Soal Asas Black
Kratos mencampur 4 kg air bersuhu 100oC dengan 8 kg air bersuhu 50oC. Berapa suhu akhir campuran?
Jawab
Diketahui:
m1 = 4 Kg
m2 = 8 Kg
c1 = c2 = c
T1 =100 oC
T2 = 50 oC
m1 = 4 Kg
m2 = 8 Kg
c1 = c2 = c
T1 =100 oC
T2 = 50 oC
Ditanyakan: Tm?
Sumber :
https://www.utakatikotak.com/kongkow/detail/15217/Kalor-Dan-Perpindahan-Kalor-Fisika-SMP-Kelas-7
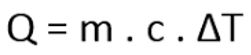
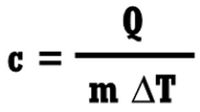

Tidak ada komentar:
Posting Komentar